Испытания любой вакцины подразумевают собственно разработку вакцины, затем доклинические исследования — на животных — и после этого три фазы клинических исследований (КИ) — на людях. Обычно в первой фазе КИ принимают участие десятки добровольцев, во второй фазе — сотни, а в третьей — тысячи и десятки тысяч. Именно третья фаза КИ позволяет дать полный ответ на вопрос об эффективности и безопасности вакцины.
Гонка фармацевтов: производители вакцин от Covid-19 наперебой заявляют о невероятной эффективности своих препаратов. Но что это значит на самом деле?
Что означает третья фаза клинических исследований
Главное, что нужно знать сейчас: на данный момент нет ни одной вакцины, по которой в научном журнале были бы опубликованы результаты третьей фазы клинических исследований. В третьей фазе КИ вакцины тестируются на тысячах добровольцев разных групп, которые формируются по возрастам, наличию или отсутствию каких-либо заболеваний. То, что какие-то вакцины (в том числе российские) уже можно использовать не в рамках исследований, отнюдь не значит, что они прошли все фазы КИ.
Временное или предварительное разрешение на использование лекарства, в том числе вакцины, — решение возможное в условиях пандемии, и для него предусмотрены соответствующие процедуры регуляторных органов (Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), Европейского агентства лекарственных средств (EMA). В данный момент временную / предварительную / ограниченную регистрацию получили две российские вакцины и четыре китайские (две из них разрешены к использованию на территории Китая, а другие две — на территории ОАЭ).
Временная регистрация «Гам-КОВИД-Вак» и «Гам-КОВИД-Вак-Лио» (они же «Спутник V»; представляют собой, по сути, одну и ту же вакцину в разных формах — в виде раствора или лиофилизата для приготовления раствора) вызвала довольно бурный негативный отклик в западных СМИ. Однако и те производители, которые получают скорее положительную оценку в медиа, тоже не пренебрегают ускоренной регистрацией своих вакцин: так, 20 ноября Pfizer заявила о том, что компания подала запрос на экстренное использование своей вакцины, а Moderna и AstraZeneca заявили о намерении подать такой запрос.

Чем отличаются вакцины
Вакцины Pfizer/BioNTech и Moderna представляют собой мРНК-вакцины. Их суть заключается в том, что фрагмент матричной РНК (мРНК) SARS-CoV-2 кодирует спайковый, или шиповидный, белок коронавируса. После того как этот фрагмент попадает в клетки, они начинают производить спайковый белок, что вызывает иммунный ответ. Фрагмент мРНК помещен в защитную липидную оболочку, которая разрушается при комнатной температуре, что требует заморозки вакцины. Для вакцины Pfizer/BioNTech требуется –70 °C, а вакцину Moderna можно хранить при –20°C. Чтобы в клинике можно было хранить вакцину Pfizer/BioNTech, там должна иметься специальная дорогостоящая низкотемпературная морозильная камера, что несколько затрудняет процесс вакцинации, особенно если речь идет об отдаленном регионе.
Вакцины «Спутник V» относятся к векторным вакцинам, которые тоже кодируют спайковый белок, только у векторных вакцин есть основа, или вектор, а именно другой вирус. Вектор специально сконструирован так, чтобы он не мог размножаться, однако когда вектор попадает в клетку, те тоже начинают производить спайковый белок. 23 ноября пресс-релиз опубликовала компания AstraZeneca, которая тоже разработала векторную вакцину. В отличие от мРНК-вакцин, векторные вакцины имеют стандартные требования к условиям хранения, а именно температуры от +2 до +8 °C.
мРНК- и векторные вакцины — это не единственный вид вакцин-кандидатов от новой коронавирусной инфекции. В России также проводятся исследования пептидной вакцины «ЭпиВакКорона» и инактивированной цельновирионной вакцины производства ФНЦИРИП им. М. П. Чумакова РАН. Пептидные вакцины содержат только отдельные белки вируса и не содержат генетического материала. Кстати, пептидная вакцина «ЭпиВакКорона» тоже получила временное регистрационное удостоверение, как и «Гам-КОВИД-Вак». Инактивированные цельновирионные вакцины — это те, в которых вирусные частицы были сохранены целиком, но они (вирусные частицы) лишены способности заражать человека. Также есть расщепленные и субъединичные вакцины, когда для вакцины используется не целый вирион, а его часть.
«Вакцина эффективна на 90%» — что это может значить?
В пресс-релизах фармацевтических компаний, которые начали выходить один за другим, заявляется об эффективности вакцин от 90%. В результате иногда даже предпринимаются народные попытки предположить разные количественные параметры, которые могли привести к тем или иным заявлениям об эффективности.
Для слова «эффективность» в отношении лекарств и вакцин, в частности, в английском языке используется три термина: efficacy, effectiveness, cost-effectiveness. Первый термин означает эффективность вакцины в идеальных условиях. Наряду с безопасностью именно идеальная эффективность является одним из основных параметров вакцины в третьей фазе клинических исследований. Однако на этом этапе еще ничего не известно об эффективности вакцины в реальных условиях (effectiveness), которую также называют действенностью. Так, предположительно серьезные требования к хранению мРНК-вакцин могут отрицательно повлиять на реальную эффективность. Наконец, третий термин, cost-effectiveness, означает экономическую эффективность, которая является важным показателем для государственных органов, принимающих решение о том, включать ли вакцинацию от какой-либо инфекции в календарь, оплачивать ли ее из средств бюджета, предоставлять по страховке или нет.
Для того чтобы оценить и сравнить эффективность каких-либо вакцин в реальных условиях, необходимо, во-первых, задать набор исходов, для которых эта эффективность будет вычисляться. У одной и той же вакцины эффективность в предотвращении случая заболевания может быть одной, а в предотвращении смерти от этого заболевания — совсем другой. Также все это может отличаться для разных групп прививаемых. Так, в исследовании четырехвалентной вакцины против гриппа, когда прививали будущих матерей, эффективность вакцинации в реальных условиях составила 72% в предотвращении гриппа, подтвержденного анализом, и 87% — в предотвращении госпитализации в связи с гриппом.
В пресс-релизах нет конкретной информации ни по набору исходов, ни по набору групп, нет конкретных чисел. Они могут содержать информацию о количестве участников, получивших вакцину по одной схеме, и количестве участников, получивших вакцину по другой схеме. В другом пресс-релизе может быть дана информация о количестве заболевших без распределения по тестовой группе (получавшей вакцину) и контрольной (получавшей плацебо). При этом, как правило, информация дается либо в целом, либо по какой-то одной группе.
Для каждой комбинации исхода в какой-либо группе необходимо знать четыре числа:
- сколько человек было в группе, получившей вакцину;
- сколько человек было в группе, получившей плацебо;
- сколько человек из группы вакцины заболели, обратились к врачу, были госпитализированы, умерли, принимали антибиотики и т. д. (это собственно исходы);
- сколько человек сделали всё то же самое из группы плацебо.
Наконец, для полноценного сравнения необходимы данные о методологии исследования, которые вовсе не указываются в пресс-релизах.
Есть ли смысл в вакцинации, если вирус мутирует?
Все вирусы так или иначе меняются, и SARS-CoV-2 не является исключением. Важным должно быть то, насколько меняется вирус и имеет ли это какие-либо клинические последствия — то есть важные в плане симптомов заболевания и для лечения, — а также то, имеет ли это последствия для производства вакцин. Исследования SARS-CoV-2 показывают, что вирус имеет низкую изменчивость и что наличие разных штаммов вируса (напомним, это является нормой) не должно стать проблемой для вакцин-кандидатов. Работа, в которой заявляется о штаммах, ускользающих от нейтрализующих антител, является препринтом, то есть она опубликована предварительно, до рецензии. В результате рецензии научная работа может быть отправлена на доработку или вовсе отклонена.
Антител может не быть после болезни. Как тогда поможет вакцина?
После перенесенной инфекции или прививки остаются антитела. Их концентрация со временем снижается. В конце концов антитела могут исчезнуть вовсе. Но это не значит, что организм будет беззащитен перед инфекцией. Иммунный ответ не ограничивается лишь тем, что у переболевшего или привитого вырабатываются специфические антитела. Иммунный ответ — это также и активация B- и T-клеток памяти, которые становятся специфичными для определенной инфекции. Если в ответ на инфекцию или прививку выработался клеточный иммунитет, то у организма осталась способность вырабатывать антитела. И в этом случае (при наличии клеточного иммунитета) при встрече с инфекцией специфические клетки памяти запускают выработку антител, чтобы побороть инфекцию. Кроме того, один из типов T-клеток, а именно CD8+ T-клетки, сам убивает инфицированные клетки организма.
В резюме комментария, вышедшего в Nature, заявляется следующее: «Недавние сообщения о том, что антитела к SARS-CoV-2 не обнаруживаются в крови после выздоровления от COVID-19, вызвали настороженность. Однако отсутствие специфических антител в крови еще не означает отсутствия иммунологической памяти. Здесь мы обсуждаем актуальные представления об относительном вкладе B- и T-клеток в иммунитет против SARS-CoV-2 и их значение для разработки эффективного лечения и вакцин от COVID-19».
Мы пока не знаем, что именно будет играть роль в предотвращении случаев повторного заражения. Впрочем, в недавнем исследовании, опубликованном в Nature, заявляется о длительном Т-клеточном иммунитете к структурному белку (не путать со спайковым белком, о котором речь шла выше).
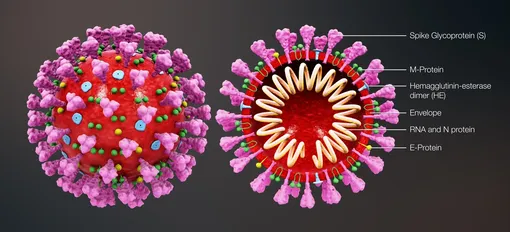
Spike glycoprotein (S) — спайковый, или шиповидный, гликопротеин S
M-protein — мембранный белок M
Hemagglutinin-esterase dimer (HE) — димер гемагглютинин-эстеразы
Envelope — оболочка
RNA and N protein — РНК- и нуклеокапсидный, или структурный, белок N
E-protein — белок оболочки E
Почему фармацевтические компании публикуют пресс-релизы раньше, чем в научных рецензируемых журналах выходят результаты клинических исследований?
Для пресс-релизов нет таких стандартов, которые существуют для научных публикаций. В исследовании необходимо детально описать запланированный дизайн и то, насколько удалось его реализовать, результаты с подробными данными по всем группам участников. Пресс-релиз же может быть каким угодно. Кроме того, чтобы любое исследование попало в научный рецензируемый журнал, оно, как следует из определения, должно пройти рецензию, которая обычно занимает несколько месяцев. Поэтому первая причина, по которой пресс-релизы появляются раньше публикаций в научных журналах, — это просто разные трудозатраты.
Есть, скорее всего, также и финансовая сторона вопроса. 9 ноября — в день, когда Pfizer выпустила пресс-релиз с информацией об эффективности, — акции компании выросли на 15% (акции партнера BioNTech выросли на 25%). В этот же день генеральный директор Pfizer в соответствии с изначальным планом продал 62% принадлежавших ему акций компании.
Наконец, учитывая хронологию и общественный интерес к вакцинам от COVID-19, нельзя исключать такой вариант, что заявления для СМИ делаются как бы в ответ на заявления конкурента.
Публикация пресс-релиза — это бизнес-составляющая процесса создания вакцины, которая не имеет отношения к науке. Именно поэтому какие-либо выводы стоит делать не раньше, чем для всех интересующих вакцин будут опубликованы результаты третьей фазы клинических исследований.
